Santé : l’anticancéreux Tazverik retiré du marché pour des raisons de sécurité
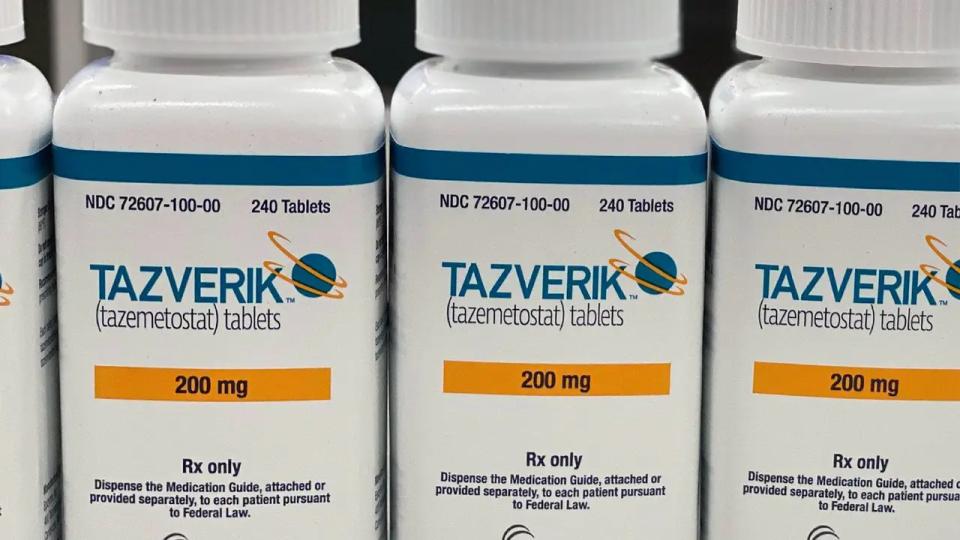
Le laboratoire pharmaceutique français Ipsen a annoncé le retrait immédiat de son médicament anticancéreux Tazverik (tazémétostat). L’information a été rendue publique dans un communiqué publié le 9 mars 2026. Cette décision fait suite à l’apparition d’effets indésirables graves observés chez certains patients lors de l’administration du traitement, notamment des cas de tumeurs malignes hématologiques secondaires, c’est-à-dire de nouveaux cancers du sang apparus pendant le traitement.
Bien que le médicament n’ait pas été commercialisé en France ni dans le reste de l’Europe, certains patients atteints de cancers rares ou difficiles à traiter ont pu en bénéficier dans le cadre d’essais cliniques ou de dispositifs d’accès précoce. Selon le laboratoire, ces nouvelles données de sécurité montrent que le rapport bénéfice-risque du médicament est désormais défavorable. Face à cette situation, Ipsen a donc choisi de procéder à un retrait volontaire du médicament et d’interrompre son utilisation afin de protéger les patients susceptibles d’y être exposés.
Un médicament utilisé dans des cas de cancers rares
L’Agence nationale de sécurité du médicament et des produits de santé (ANSM) précise que depuis le 31 août 2023, le médicament n’est plus mis à disposition dans le cadre des accès compassionnels. Depuis cette date, seuls les patients déjà sous traitement peuvent poursuivre leur prise, à condition que leur médecin estime que le bénéfice reste suffisant. En revanche, Tazverik était commercialisé aux États-Unis depuis 2020 pour le traitement de certains lymphomes folliculaires et du sarcome épithélioïde avancé ou métastatique.
Les résultats d’un essai clinique mené dans 15 pays, dont les États-Unis, plusieurs pays de l’Union européenne et la Chine, ont montré que si le médicament pouvait agir chez certains patients, il n’améliore pas significativement les résultats par rapport aux traitements déjà existants. Pire encore, il exposait les malades à des effets secondaires supplémentaires. À la lumière de ces conclusions, le laboratoire a décidé d’interrompre les essais cliniques et les programmes d’accès élargis liés à ce traitement, tout en poursuivant le suivi à long terme des patients déjà inclus dans les études.










GMT TV